
一、FDA QSR 820的定义QSR是质量体系法规的简写,820实际指的是CFR 21 PART 820部分,是FDA法规中对于医疗器械质量管理体系的相关要求。 QSR820不是孤立的要求,其要求与PART 803,PART 807等其他部分都紧密相关。QSR820和ISO13485的要求有部分类似, 但又有明显的差异。二、FDA对QSR820的监控方式FDA不会像...
累计服务6000+ 好评率98.5%
一、FDA QSR 820的定义
QSR是质量体系法规的简写,820实际指的是CFR 21 PART 820部分,是FDA法规中对于医疗器械质量管理体系的相关要求。 QSR820不是孤立的要求,其要求与PART 803,PART 807等其他部分都紧密相关。QSR820和ISO13485的要求有部分类似, 但又有明显的差异。
二、FDA对QSR820的监控方式
FDA不会像CFDA一样在发放许可证之前先进行体系考核。FDA对于所有的企业的体系考核是通过后续的抽查形式来进行监控的, 全球的医疗器械注册企业都会有被抽查到的可能性。风险越高的器械的生产企业被抽查到的概率越高。通常抽查会提前两 个月通知被检查的企业,也有部分是提前一周才通知的。
三、QSR820审核的可能的结果
NAI(审核无483直接通过)
VAI(审核有483,是一般不符合)
OAI(审核有483,是严重不符合)
Warning Letter 警告信(企业必须在规定期限回复,有可能需要再次审核进行验证)
Import Alert 进口禁令(企业产品到美国海关会被自动扣留,进入DWPE程序)
四、QSR820 的要求
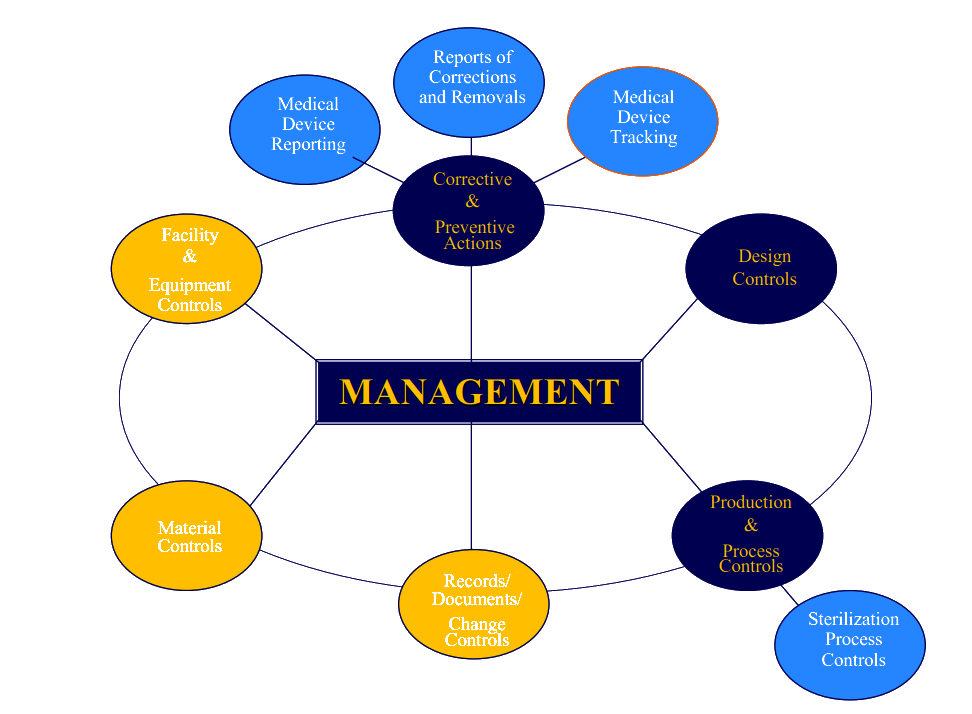
QSR820的要求分为7个子体系,分别是:管理控制、纠正和预防措施(CAPA)(具有辅助的医疗器械报告系统、纠正和移 除系统、医疗器械记录系统)、设计控制、生产和过程控制(P&PC)(具有辅助的灭菌过程控制系统)、设备设施控制、 材料控制以及文件记录和变更控制。

扫一扫加微信
手机:19866028503
电话:0769-22223610
邮箱:323714635@qq.com
地址:中国·广东省东莞市松山湖园区研发五路2号3栋414室
友情链接:
版权所有:Copyright © 2021 思誉企业管理顾问有限公司 版权所有 备案号:粤ICP备17098289号-1